中山大学张锐团队开发具有独立知识产权的可灵活裁剪RNA的编辑技术
(通讯员张锐)在生命科学领域,基因编辑技术的每一次革新都深刻影响着疾病治疗的未来。近年来,随着基因编辑技术的迅速发展,RNA编辑作为一种新兴的治疗方法,受到了科学界和产业界的广泛关注。与传统的DNA编辑相比,RNA编辑避免了对遗传信息的永久改变,具有可逆性和可控性,极大地提高了基因编辑技术的安全性。但现有的RNA编辑技术大多集中在单碱基编辑领域,限制了RNA编辑的临床应用场景。
近日,中山大学生命科学学院张锐教授课题组在《Molecular Cell》上发表了题为“Type III CRISPR-mediated flexible RNA excision with engineered guide RNAs”的研究论文,报道了一项重要的技术突破——一种名为SCISSOR(Selective Cleavage and Intramolecular Stitching of RNA)的RNA编辑工具,使我们首次能够在RNA层面进行灵活的裁剪和改变读码框。这一技术突破不仅填补了现有RNA编辑领域的空白,更为各类移码突变导致的遗传疾病和肿瘤免疫治疗提供了全新的解决方案。据悉,该研究成果也被选为Molecular Cell 3月6日出版当期的封面论文重点推荐。
SCISSOR工具的核心突破在于其独特的“凸起环”设计,这一创新性设计赋予了III型 CRISPR-Csm复合物在RNA编辑过程中前所未有的灵活性和多样性。传统上,CRISPR-Csm系统介导的RNA编辑中存在很大的局限性,只能以 6nt的倍数进行RNA片段的删除。SCISSOR通过引入“凸起环”设计,让 Csm 系统突破6nt倍数限制,可对RNA进行任意长度小片段删除,并精准调整开放阅读框(ORF),实现移码突变的修复。
为了评估SCISSOR在修复移码突变中的治疗潜力,张锐实验室靶向了HEXA基因中的一个临床相关的移码突变。该突变是HEXA基因外显子上一个4个碱基(TATC,1278ins4)的插入突变,是引起泰-萨克斯病(TSD)最常见的突变,约占所有TSD病例的80%。研究中,团队利用SCISSOR技术成功修复了这一移码突变,标志着历史上首次通过RNA切割的方式直接修正蛋白编码基因中的致病移码突变。
SCISSOR的能力不仅限于“修复”,还可通过人为引入移码突变,因此在癌症免疫治疗中的应用也显示出其独特的潜力。通过SCISSOR平台,研究人员能够靶向肿瘤高表达或者特异表达的促癌基因引入移码突变,生成具有高度免疫原性的多肽。因此SCISSOR可以跟mRNA疫苗联用,创造全新的通用型肿瘤免疫疫苗治疗策略,具有潜在的广泛应用前景。
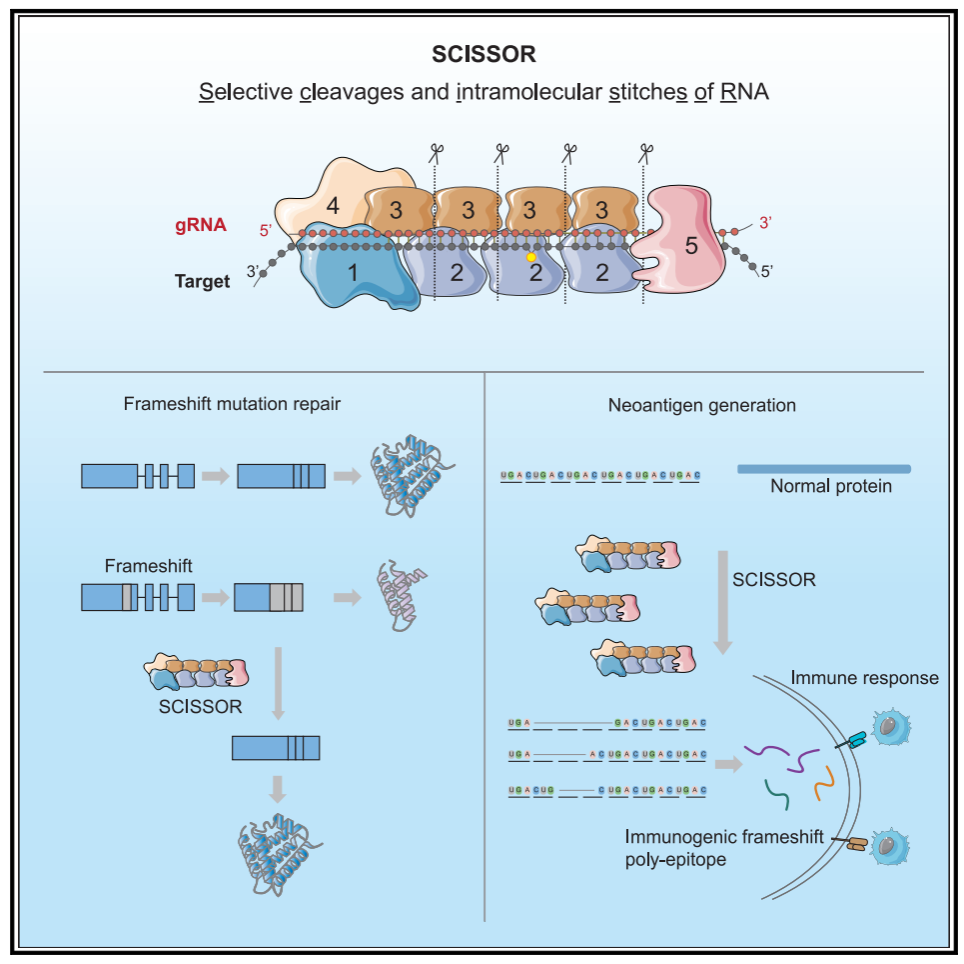
总的来说,SCISSOR技术不仅填补了现有RNA编辑领域的空白,也为各类移码突变导致的遗传疾病和肿瘤免疫治疗提供了全新的解决方案。虽然面临一些技术挑战,但随着研究的持续推进,SCISSOR有望成为RNA编辑领域的核心技术之一,为基因治疗、肿瘤免疫治疗等领域带来前所未有的突破。
作为一项具有独立知识产权的颠覆性RNA编辑技术,SCISSOR已经布局了中国发明专利和PCT国际专利,具有广阔的临床转化前景。
张锐团队博士研究生孙远帆、吴英尹,硕士研究生何梓华、王燚莹及侯文豪为该论文的并列第一作者,张锐为通讯作者,张锐团队博士研究生曹勇、周琪皓也对本工作做出贡献。该研究得到了国家重点研发专项、广州市基础与应用基础研究专题科技菁英“领航”项目和广州市科学技术局重点研发计划的资助。
论文链接:
https://www.cell.com/molecular-cell/fulltext/S1097-2765(25)00055-3
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...