中山大学王金凯课题组开发深度学习算法揭示m6A在RNA异构体上的复杂性
(通讯员郭文冰、王金凯)真核生物的pre-mRNA能够通过选择性加工形成不同的RNA异构体,这些可变的加工方式包括可变剪接、可变加尾,此外,相同基因也存在可变启动子,从而产生具有不同5’端的RNA异构体。这些种类复杂的RNA异构体在哺乳动物细胞中广泛存在,然而m6A是否能够选择性地标记这些RNA异构体并不清楚,尤其是不同RNA异构体上的相同m6A位点是否也能够产生差异的m6A修饰?对这一科学问题理解的欠缺主要是由于技术的匮乏。
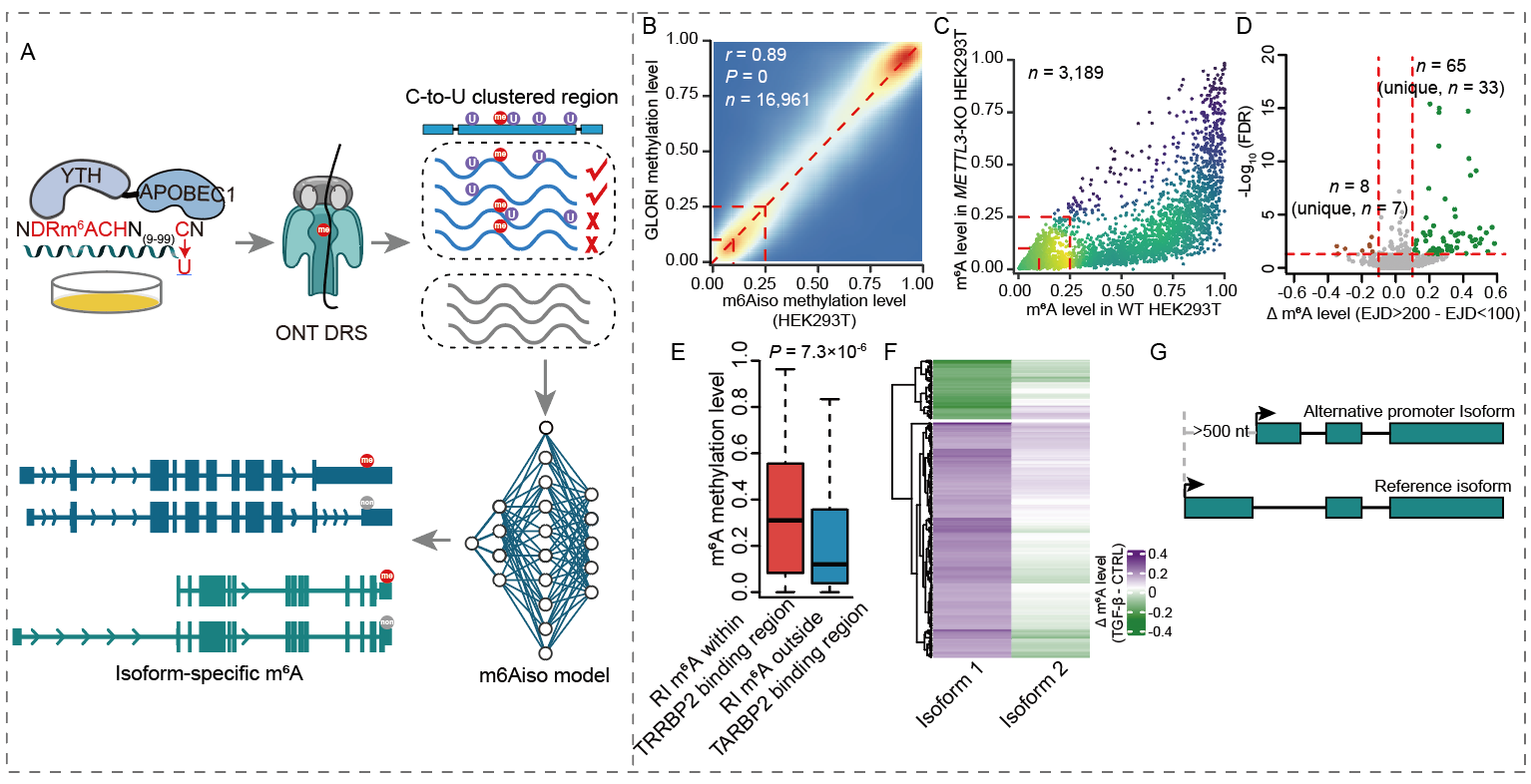
2025年2月7日,中山大学中山医学院王金凯课题组在Molecular Cell杂志上在线发表了题为“Single-molecule m6A detection empowered by endogenous labeling unveils complexities across RNA isoforms”的研究论文。该论文通过APOBEC1-YTH在细胞内使内源的RNA的m6A附近产生C-to-U突变并进行第三代牛津纳米孔直接RNA测序(ONT DRS),从而通过已知m6A位点附近10~100 nt的C-to-U突变在单分子水平对m6A进行内源性标记,通过半监督学习进行数据清洗后,获得约一百万个单分子水平的5-mer的m6A电信号,训练出一个在单分子水平准确检测m6A修饰的深度学习模型m6Aiso。进而揭示了相同的m6A位点在不同的异构体上也能够通过至少三种不同的机制产生广泛的差异。尤其是在上皮间质转化模型中,TGF-β诱导后,活化的转录因子SMAD3会通过招募METTL3/METTL14/WTAP选择性地促进以SMAD3为启动子的下游RNA的m6A修饰, 从而造成相同基因使用不同启动子的异构体呈现选择性的m6A上调。该研究为理解m6A在异构体上的复杂性以及m6A的选择性调控机理提供了新的视角。
该研究论文通讯作者是中山大学中山医学院王金凯教授,其课题组博士后郭文冰、任志军和黄翔为论文的共同第一作者。该工作得到国家自然科学基金、广东省科学基金、博士后基金以及中山大学学科交叉团队项目的支持。
论文链接:https://www.cell.com/molecular-cell/abstract/S1097-2765(25)00049-8
© 版权声明
本文由分享者转载或发布,内容仅供学习和交流,版权归原文作者所有。如有侵权,请留言联系更正或删除。
相关文章

暂无评论...